Проницаемость и проводимость клеточной мембраны. Липидные поры: стабильность и проницаемость мембран
Читайте также
3.3. Мембранный потенциал покоя
3.3.1. Общая характеристика и непосредственная причина формирования
Потенциал покоя (1111) - разность электрических потенциалов между наружной и внутренней сторонами клеточной мембраны. Его
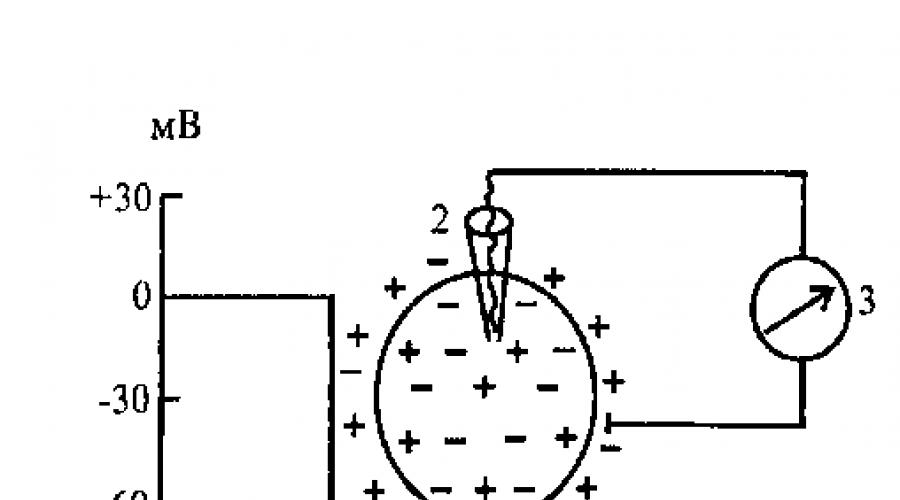
величина в нервных клетках составляет 60-80 мВ. При регистрации ПП луч осциллографа во время прокола мембраны клетки микроэлектродом скачком отклоняется и показывает отрицательный заряд внутри клетки (рис. 3.1).
ПП играет исключительно важную роль в жизнедеятельности самого нейрона и организма в целом. В частности, он составляет основу для перера ботки информации в нервной клетке, обеспечивает регуляцию деятельности внутренних органов и опорно-двигательного аппарата посредством запуска процессов возбуждения и сокращения в мышце. Согласно мембранно-ионной теории (Бернштейн, Ходжкин, Хаксли, Катц), непосредственной причиной формирования ПП является неодинаковая концентрация анионов и катионов внутри и вне клетки (табл. 3.1).

В нейронах концентрация ионов К + внутри клетки в 20-40 раз больше, чем вне клетки; концентрация ионов Na + вне клетки в 10-12 раз больше, чем в клетке. Ионов СГ вне клетки в 10-20 раз больше, чем внутри клетки. В клетке имеется небольшое количество ионов Mg 2+ . Ион Са 2+ в клетке находится в основном в связанном состоянии с АТФ, цитратом, глутаматом. Резервуаром для ионов Са 2+ является эндоплазматический ретику-лум. В свободном состоянии кальций находится в основном вне клетки; в гиалоплазме его
очень мало. Это обусловлено отчасти активным транспортом ионов Са 2+ наружу через клеточную мембрану, отчасти поглощением его эндоплазматическим ретикулумом и другими органеллами, например митохондриями. В клетке находятся также крупномолекулярные анионы, главным образом это отрицательно заряженные белковые молекулы, например глутамат, аспартат, а также органические фосфаты. Различные ионы распределены неравномерно по обе стороны клеточной мембраны, во-первых, вследствие неодинаковой проницаемости клеточной мембраны для различных ионов, во-вторых, в результате работы ионных насосов, транспортирующих ионы в клетку и из клетки вопреки концентрационному и электрическому градиентам. По поводу определения «проницаемость» и «проводимость» единого мнения пока не сложилось.
3.3.2. Роль проницаемости клеточной мембраны и ее поверхностных зарядов
А. Терминология. В настоящее время различные авторы по-разному трактуют термины «проницаемость» и «проводимость». Под проницаемостью клеточной мембраны мы понимаем ее способность пропускать воду и частицы - заряженные (ионы) и незаряженные согласно законам диффузии и фильтрации. Проницаемость клеточной мембраны определяется следующими факторами: 1) наличием в составе мембраны различных ионных каналов -управляемых (с воротным механизмом) и неуправляемых (каналы утечки); 2) размерами каналов и размерами частиц; 3) растворимостью частиц в мембране (клеточная мембрана проницаема для растворимых в ней липидов и непроницаема для пептидов).
Термин «проводимость» следует использовать только применительно к заряженным частицам. Следовательно, под проводимостью мы понимаем способность заряженных частиц (ионов) проходить через клеточную мембрану согласно электрохимическому градиенту (совокупность электрического и концентрационного градиентов).
Как известно, ионы, подобно незаряженным частицам, переходят через мембрану из области с высокой концентрацией в область с низкой концентрацией. При большом градиенте концентрации и хорошей проницаемости мембраны, разделяющей соответствующие растворы, проводимость ионов может быть высокая, при этом наблюдается односторонний ток ионов. Когда концентрация ионов по обе стороны мембраны уравняется, проводимость ионов уменьшится, односторонний ток ионов прекратится, хотя проницаемость сохранится прежней - высокой. Кроме того, проводимость иона при неизменной проницаемости мембраны зависит и от заряда иона: одноименные заряды отталкиваются, разноименные притягиваются, т.е. важную роль в проводимости иона играет его электрический заряд. Возможна ситуация, когда при хорошей проницаемости мембраны проводимость ионов через мембрану оказывается низкой или нулевой, - в случае отсутствия движущей силы (концентрационного и /или электрического градиентов).
Таким образом, проводимость иона зависит от его электрохимического градиента и от проницаемости мембраны: чем они больше, тем лучше проводимость иона через мембрану. Перемещения ионов в клетку и из клетки согласно концентрационному и электрическому градиентам в состоянии покоя клетки осуществляются преимущественно через неуправляемые (без воротного механизма) каналы (каналы утечки). Неуправляемые каналы всегда открыты, они практически не меняют своей пропускной способности при электрическом воздействии на клеточную мембрану и ее возбуждении. Неуправляемые каналы подразделяются на ионоселек-тивные каналы (например, калиевые медленные неуправляемые каналы) и иононеселективные каналы. Последние пропускают различные ионы: К + , Na + , С1 _ .
Б. Роль проницаемости клеточной мембраны и различных ионов в формировании 1111 (рис. 3.2.). Сосуд разделен полупроницаемой мембраной. Обе его половины заполнены раствором K 2 SO 4 различной концентрации (О и С2), причем Ci < С2. Мембрана проницаема для иона К + и непроницаема для S04 2 ". Ионы К + перемещаются согласно

Ионы Na + и К + в живой клетке, находящейся в состоянии покоя, также перемещаются через мембрану согласно законам диффузии, при этом К + из клетки выходит в значительно большем количестве, чем входит Na + в клетку, поскольку проницаемость клеточной мембраны для К + примерно в 25 раз больше проницаемости для Na + .
Органические анионы из-за своих больших размеров не могут выходить из клетки, поэтому внутри клетки в состоянии покоя отрицательных ионов оказывается больше, чем по-
ложительных. По этой причине клетка изнутри имеет отрицательный заряд. Интересно, что во всех точках клетки отрицательный заряд практически одинаков. Об этом свидетельствует одинаковая величина ПП при введении микроэлектрода на разную глубину внутрь клетки, как это имело место в опытах Ходжкина, Хаксли и Катца. Заряд внутри клетки является отрицательным как абсолютно (в гиалоплазме клетки содержится больше анионов, чем катионов), так и относительно наружной поверхности клеточной мембраны.
Калий является главным ионом, обеспечивающим формирование ПП. Об этом свидетельствуют результаты опыта с перфузией внутреннего содержимого гигантского аксона кальмара солевыми растворами. При уменьшении концентрации ионов К + в перфуза-те ПП снижается, при увеличении их концентрации ПП повышается. В состоянии покоя клетки устанавливается динамическое равновесие между числом выходящих из клетки и входящих в клетку ионов К + . Электрический и концентрационный градиенты противодействуют друг другу: согласно концентрационному градиенту К + стремится выйти из клетки, отрицательный заряд внутри клетки и положительный заряд наружной поверхности клеточной мембраны препятствуют этому. Когда концентрационный и электрический градиенты уравновесятся, число выходящих из клетки ионов К + сравнивается с числом входящих ионов К + в клетку. В этом случае на клеточной мембране устанавливается так называемый равновесный потенциал.
Равновесный потенциал для иона можно рассчитать по формуле Нернста. Концентрация положительно заряженного иона, находящегося снаружи, в формуле Нернста записывается в числителе, а иона, находящегося внутри клетки, - в знаменателе. Для отрицательно заряженных ионов расположение противоположное.
Е _ЛГ . 1п М,
~~ ZF [ ion \ "
где Е- тп - потенциал, создаваемый данным ионом; R - газовая постоянная (8,31 Дм); Т - абсолютная температура (273+37°С); Z -валентность иона; F - постоянная Фарадея (9,65 х 10 4); [гол],- - концентрация иона внутри клетки inside; [ ion ] 0 - концентрация иона во внешней среде клетки outside. Равновесный потенциал иона Na + у нервных клеток Еы я - +55 мВ, иона калия Ек - -70 мВ.
Вклад Na + и С1~ в создание ПП. Проницаемость клеточной мембраны в покое для иона Na + очень низкая, намного ниже, чем для иона К + , тем не менее она имеется, поэтому ионы Na + согласно концентрационному и электрическому градиентам стремятся и в небольшом количестве проходят внутрь клетки. Это ведет к уменьшению ПП, так как на внешней поверхности клеточной мембраны суммарное число положительно заряженных ионов уменьшается, хотя и незначительно, а часть отрицательных ионов внутри клетки нейтрализуется входящими в клетку положительно заряженными ионами Na + . Вход иона Na + внутрь клетки снижает ПП. Влияние СГ на величину ПП противоположно и зависит от проницаемости клеточной мембраны для ионов СГ. Дело в том, что ион СГ, согласно концентрационному градиенту, стремится и проходит в клетку. Препятствует входу иона СГ в клетку электрический градиент, по скольку заряд внутри клетки отрицательный, как и заряд СГ. На ступает равновесие сил концентрационного градиента, способствующего входу иона СГ в клетку, и электрического градиента, препятствующего входу иона СГ в клетку. Поэтому внутриклеточная концентрация ионов СГ значительно меньше внеклеточной. При поступлении иона СГ внутрь клетки число отрицательных зарядов вне клетки несколько уменьшается, а внутри клетки увеличивается: ион СГ добавляется к крупным, белковой природы анионам, находящимся внутри клетки. Эти анионы из-за своих больших размеров не могут пройти через каналы клеточной мембраны наружу клетки - в интерстиций. Таким образом, ион СГ, проникая внутрь клетки, увеличивает ПП. Частично, как и вне клетки, ионы Na + и С1~ внутри клетки нейтрализуют друг друга. Вследствие этого совместное поступление ионов Na + и С1~ внутрь клетки не сказывается существенно на величине ПП.
В. Определенную роль в формировании ПП играют поверхностные заряды самой клеточной мембраны и ионы Са 2+ . Наружная и внутренняя поверхности клеточной мембраны несут собственные электрические заряды, преимущественно с отрицательным знаком. Это полярные молекулы клеточной мембраны: гликолипиды, фосфолипиды, гликопротеиды. Фиксированные наружные отрицательные заряды, нейтрализуя положительные заряды внешней поверхности мембраны, снижают ПП. Фиксированные внутренние отрицательные заряды клеточной мембраны, напротив, суммируясь с анионами внутри клетки, увеличивают ПП.
Роль ионов Са 2+ в формировании ПП заключается в том, что они взаимодействуют с наружными отрицательными фиксированными зарядами мембраны клетки и нейтрализуют их, что ведет к увеличению и стабилизации ПП.
Таким образом, ПП - это алгебраическая сумма не только всех зарядов ионов вне и внутри клетки, но также алгебраическая сумма отрицательных внешних и внутренних поверхностных зарядов самой мембраны.
При проведении измерений потенциал окружающей клетку среды принимают равным нулю. Относительно нулевого потенциала внешней среды потенциал внутренней среды нейрона, как отмечалось, составляет величину порядка -60-80 мВ. Повреждение клетки приводит к повышению проницаемости клеточных мембран, в результате чего различие проницаемости для ионов К + и Na + уменьшается, ПП при этом снижается. Подобные изменения встречаются при ишемии ткани. У сильно поврежденных клеток ПП может снизиться до уровня донанновского равновесия, когда концентрация внутри и вне клетки будет определяться только избирательной проницаемостью клеточной мембраны в состоянии покоя клетки, что может привести к нарушению электрической активности нейронов. Однако и в норме происходит перемещение ионов согласно электрохимическому градиенту, однако ПП не нарушается.
| " |
ПРОНИЦАЕМОСТЬ - способность клеток и тканей поглощать, выделять и транспортировать химические вещества, пропуская их через клеточные мембраны, стенки сосудов и клетки эпителия. Живые клетки и ткани находятся в состоянии непрерывного обмена хим. веществами с окружающей средой. Основным барьером (см. Барьерные функции) на пути движения веществ является клеточная мембрана. Поэтому исторически механизмы П. исследовались параллельно с изучением структуры и функции биологических мембран (см. Мембраны биологические).
Различают пассивную П., активный транспорт веществ и особые случаи П., связанные с фагоцитозом (см.) и пиноцитозом (см.).
В соответствии с мембранной теорией П. в основе пассивной П. лежат различные виды диффузии вещества через клеточные мембраны (см. Диффузия
где dm - количество вещества, диффундирующего за время dt через площадь S; dc/dx - градиент концентрации вещества; D - коэффициент диффузии.
Рис. 1. Молекулярная организация ионофорного антибиотика (валиномицина): а - структурная формула молекулы валиномицина, содержащей шесть правовращающих (D) и шесть левовращающих (L) аминокислот, все боковые группы [-СН 3 -СН (СН 3) 2 ] гидрофобны; б - схематическое изображение пространственной конфигурации комплекса валиномицина с ионом калия (в центре). Часть карбонильных групп комплекса образует водородные связи с атомами азота, а другие - координационные связи с катионом (ионом калия). Гидрофобные группы формируют внешнюю гидрофобную сферу комплекса и обеспечивают его растворимость в углеводородной фазе мембраны; 1 - атомы углерода, 2 - атомы кислорода, 3 - катион (ион калия), 4- атомы азота, 5 - водородные связи, 6 - координационные связи. Ион калия, «захваченный» молекулой валиномицина, переносится этой молекулой через мембрану клетки и высвобождается. Таким путем обеспечивается избирательная проницаемость клеточной мембраны для ионов калия.
При исследовании П. клетки для растворенного вещества вместо градиента концентрации употребляют понятие разности концентраций диффундирующего вещества по обе стороны мембраны, а вместо коэффициента диффузии - коэффициент проницаемости (Р), зависящий также от толщины мембраны. Одним из возможных путей проникновения веществ в клетку является растворение их в липидах клеточных мембран, что подтверждается существованием прямой пропорциональной зависимости между коэффициентом проницаемости большого класса хим. соединений и коэффициентом распределения вещества в системе масло - вода. В то же время вода не подчиняется этой зависимости, скорость ее проникновения значительно выше и не пропорциональна коэффициенту распределения в системе масло - вода. Для воды и растворенных в ней низкомолекулярных веществ наиболее вероятным способом П. является прохождение через мембранные поры. Т. о., диффузия веществ через мембрану может происходить путем растворения этих веществ в липидах мембраны; путем прохождения молекул через полярные поры, образуемые полярными, заряженными группами липидов и белков, а также путем прохождения через незаряженные поры. Особыми видами являются облегченная и обменная диффузии, обеспечиваемые белками и жирорастворимыми веществами-переносчиками, которые способны связывать переносимое вещество по одну сторону мембраны, диффундировать с ним через мембрану и освобождать его по другую сторону мембраны. Скорость переноса вещества через мембрану в случае облегченной диффузии значительно выше, чем при простой диффузии. Роль специфических переносчиков ионов могут выполнять некоторые антибиотики (валиномицин, нигерицин, моненсин и ряд других), получившие название ионофорных (см. Ионофоры). Расшифрована молекулярная организация комплексов ионофорных антибиотиков с катионами. В случае валиномицина (рис. 1) показано, что после связывания с катионом калия молекула пептида изменяет конформацию, приобретая вид браслета с внутренним диаметром ок. 0,8 нм, в к-ром ион калия удерживается в результате ион-дипольных взаимодействий.
Распространенным видом пассивной П. клеточных мембран для полярных веществ является П. через поры. Хотя непосредственное наблюдение пор в липидном слое мембраны представляет трудную задачу, экспериментальные данные свидетельствуют об их реальном существовании. В пользу реального существования пор свидетельствуют также данные об осмотических свойствах клеток. Величина осмотического давления в растворах, окружающих клетку, может быть рассчитана по формуле:
π=σ CRT,
где π - осмотическое давление; С - концентрация растворенного вещества; R - газовая константа; Т - абсолютная температура; σ - коэффициент отражения. Если скорость прохождения через мембрану молекулы растворенного вещества соизмерима со скоростью прохождения молекул воды, то величины сил будут близки к нулю (осмотическое изменение объема клетки отсутствует); если клеточная мембрана непроницаема для данного вещества, то величина σ стремится к 1 (осмотическое изменение объема клетки максимально). Скорость проникновения молекул через клеточную мембрану зависит от размеров молекулы и, таким образом, путем подбора молекул определенного размера и наблюдения за изменением объема клеток в растворе данного вещества можно определить размеры клеточных пор. Напр., мембрана аксона кальмара слабопроницаема для молекул глицерина, имеющих в радиусе ок. 0,3 нм, но проницаема для веществ с меньшими размерами молекул (табл.). Аналогичные эксперименты с другими клетками показали, что размеры пор в клеточных мембранах, в частности в мембранах эритроцитов, кишечной палочки, клеток эпителия кишечника и др., достаточно точно укладываются в пределах 0,6-0,8 нм.
Для живых клеток и тканей характерен и другой способ проникновения веществ в клетку и выхода из нее - активный транспорт веществ. Активный транспорт - это перенос вещества через клеточную (или внутриклеточную) мембрану (трансмембранный активный транспорт) или через слой клеток (трансцеллюлярный активный транспорт), протекающий против электрохимического градиента (см. Градиент). т. е. с затратой свободной энергии организма (см. Обмен веществ и энергии). Молекулярные системы, отвечающие за активный транспорт веществ, находятся в клеточной (или внутриклеточной) мембране. В цитоплазматических мембранах клеток, участвующих в активном транспорте ионов,- мышечных клетках, нейронах, эритроцитах, клетках почек - в значительных количествах находится фермент Na+, Независимая АТФ-аза, активно участвующий в механизмах переноса ионов (см. Транспорт ионов). Механизм функционирования этого фермента наиболее изучен на эритроцитах и аксонах, обладающих ярковыраженной способностью накапливать ионы калия и удалять (откачивать) ионы натрия. Предполагается, что эритроциты содержат молекулярное устройство - калиево-натриевый насос (калий-натриевая помпа), обеспечивающее избирательное поглощение ионов калия и избирательное удаление из клетки ионов натрия, а основным элементом этого насоса является Na + , К + -АТФ-аза. Изучение свойств фермента показало, что фермент активен только в присутствии ионов калия и натрия, причем ионы натрия активируют фермент со стороны цитоплазмы, а ионы калия - со стороны окружающего раствора. Специфическим ингибитором фермента является сердечный гликозид уабаин. Обнаружены и другие транспортные АТФ-азы, в частности, транспортирующие ионы Са +2 .
В мембранах митохондрий известна молекулярная система, обеспечивающая откачку ионов водорода,- фермент Н + -АТФ-аза, а в мембранах саркоплазматического ретикулума - фермент Са ++ -АТФ-аза. Митчелл (P. Mitchell) - автор хемиосмотической теории окислительного фосфорилирования в митохондриях (см. Фосфорилирование) - ввел понятие «вторичный транспорт веществ», который осуществляется за счет энергии мембранного потенциала и (или) градиента pH. Если для ионных АТФ-аз противоградиентное перемещение ионов и утилизация АТФ обеспечиваются одной и той же ферментной системой, то в случае вторичного активного транспорта эти два события обеспечиваются разными системами и могут быть разделены во времени и пространстве.
Проникновение в клетки крупных макромолекул белка, нуклеиновых к-т. клеточных ферментов и целых клеток осуществляется по механизму фагоцитоза (захвата и поглощения клеткой крупных твердых частиц) и пиноцитоза (захвата и поглощения частью клеточной поверхности окружающей жидкости с растворенными в ней веществами).
П. клеточных мембран имеет больше значение для функционирования клеток и тканей.
Активный транспорт ионов и сопутствующее ему поглощение воды в клетках почечного эпителия происходит в проксимальных канальцах почки (см. Почки). Через почки взрослого человека ежедневно проходит до 1800 л крови. Белки при этом отфильтровываются и остаются в крови, 80% солей и воды, а также вся глюкоза поступают обратно в кровяное русло. Считается, что первопричиной этого процесса является трансцеллюлярный активный транспорт ионов натрия, обеспечиваемый Na+ K+-зависимой АТФ-азой, локализованной в клеточных мембранах базального эпителия. Если в русле почечного проксимального канальца концентрация ионов натрия составляет ок. 100 ммоль/л, то внутри клетки она не превышает 37 ммолъ/л; вследствие этого пассивный поток ионов натрия направлен внутрь клетки. Пассивному проникновению катионов в цитоплазму способствует также наличие мембранного потенциала (внутренняя поверхность мембраны заряжена отрицательно). Т. о. внутрь клетки ионы натрия проникают пассивно в соответствии с концентрационным и электрическим градиентами (см. Градиент). Выход же ионов из клетки в плазму крови осуществляется против концентрационного и электрического градиентов. Установлено, что именно в базальной мембране и локализован натрий-калиевый насос, обеспечивающий удаление ионов натрия. Предполагается, что анионы хлора движутся вслед за ионами натрия по межклеточному пространству. В результате этого осмотическое давление плазмы крови возрастает, и вода из русла канальца начинает поступать в плазму крови, обеспечивая реабсорбцию соли и воды в почечных канальцах.
Для изучения пассивной и активной П. используются различные методы. Значительное распространение получил метод меченых атомов (см. Изотопы , Радиоактивные препараты , Радиоизотопное исследование). Для изучения ионной П. клеток используются изотопы 42 K, 22 Na и 24 Na, 45 Ca, 86 Rb, 137 Cs, 32 P и др.; для изучения П. воды - дейтериевая или тритиевая вода, а также вода, меченная по кислороду (18O); для изучения П. сахаров и аминокислот - соединения, меченные по углероду 14 C или сере 35 S; для изучения П. белков - иодированные препараты, меченные по 1 31 I.
Широко применяются при исследовании П. витальные красители. Сущность метода заключается в наблюдении под микроскопом скорости проникновения молекул красителя внутрь клетки. Для большинства витальных красителей (нейтральный красный, метиленовый синий, родамин и др.) наблюдения проводятся в видимой части спектра. Используются также флюоресцирующие соединения, и среди них флюоресцеин натрия, хлортетрациклин, мурексид и др. При исследовании мышц было показано, что П. молекул красителей зависит не только от свойств клеточной мембраны, но и от сорбирующей способности внутриклеточных структур, чаще всего белков и нуклеиновых к-т, с к-рыми красители связываются.
Для изучения П. воды и растворенных в ней веществ применяют осмотический метод. При этом с помощью микроскопа или измерения светорассеяния суспензии частиц наблюдают за изменением объема клеток в зависимости от тоничности окружающего р-ра. Если клетка находится в гипертоническом р-ре, то вода из нее переходит в раствор и клетка сжимается. Противоположный эффект наблюдается в гипотоническом р-ре.
Все чаще для изучения П. клеточных мембран применяют потенциометрические методы (см. Микроэлектродный метод исследования , Электропроводность биологических систем); широкий набор ионоспецифичных электродов позволяет исследовать кинетику транспорта многих неорганических ионов (калия, натрия, кальция, водорода и др.), а также некоторых органических ионов (ацетатов, салицилатов и др.). Все виды П. клеточных мембран в той или иной степени характерны для многоклеточных тканевых мембранных систем - стенок кровеносных сосудов, эпителия почек, слизистой оболочки кишечника и желудка. Вместе с тем для П. сосудов характерны некоторые особенности, проявляющиеся в нарушении сосудистой П. (см. ниже).
Патологическая физиология сосудистой проницаемости
Термином «сосудистая проницаемость» пользовались для обозначения гистогематического и транскапиллярного обмена, распределения веществ между кровью и тканями, тканевой П., гемолимфатического перехода веществ и других процессов. Некоторые исследователи применяют этот термин для обозначения трофической функции капилляро-соединительнотканных структур. Неоднозначность использования термина было одной из причин противоречивости взглядов по ряду вопросов, особенно касающихся регуляции сосудистой П. В 70-х гг. 20 в. термин «сосудистая проницаемость» стали использовать гл. обр. для обозначения избирательной проницаемости, или барьернотранспортной функции, стенок кровеносных микрососудов. Имеется тенденция к отнесению к сосудистой П. также и П. стенок не только микрососудов (кровеносных и лимфатических), но и крупных сосудов (вплоть до аорты).
Изменения сосудистой П. наблюдаются гл. обр. в форме повышения избирательной П. для макромолекул и клеток крови. Типичным примером этого является экссудация (см.). Понижение сосудистой П. связывают в основном с белковым пропитыванием и последующим уплотнением сосудистых стенок, что наблюдается, напр., при гипертонической болезни (см.).
Существует мнение о возможности нарушения П. сосудистой стенки преимущественно в направлении интерстиция или из интерстиция в кровь. Однако преимущественное движение веществ в ту или другую сторону относительно сосудистой стенки еще не доказывает его связь с состоянием барьерно-транспортной функции сосудистой стенки.
Принципы изучения нарушений сосудистой проницаемости
Оценку состояния сосудистой П. необходимо проводить с учетом того, что сосудистая стенка обеспечивает разграничение и функциональную связь двух смежных сред (крови и внутритканевой среды), являющихся основными компонентами внутренней среды организма (см.). Обмен между этими смежными средами в целом осуществляется за счет микрогемоциркуляции (см. Микроциркуляция), а сосудистая стенка с ее барьерно-транспортной функцией выступает лишь в качестве основы органной специализации гистогематического обмена. Поэтому метод изучения состояния сосудистой П. можно считать адекватным только тогда, когда он позволяет оценивать качественные параметры гистогематического обмена с учетом их органоспецифичности и независимо от состояния органной микрогемоциркуляции и характера обменных процессов, формирующихся вне сосудистой стенки. С этой точки зрения наиболее адекватным из существующих методов является электронно-микроскопический метод изучения сосудистой П., позволяющий прямым способом наблюдать пути и механизмы проникновения веществ через сосудистую стенку. Особенно плодотворным оказалось сочетание электронной микроскопии с так наз. трассирующими индикаторами, или трейцерами, метящими пути своего движения через сосудистую стенку. В качестве таких индикаторов могут быть использованы любые нетоксические вещества, выявляемые с помощью электронной микроскопии или специальных приемов (гистохимически, радиоавтографически, иммуноцитохимически и др.). С этой целью применяют железосодержащий белок ферритин, различные ферменты с пероксидазной активностью, коллоидный уголь (очищенную черную тушь) и т. д.
Из непрямых методов изучения состояния барьерно-транспортной функции стенок кровеносных сосудов наиболее широкое распространение получила регистрация проникновения через сосудистую стенку естественных или искусственных индикаторов, слабо или вообще не проникающих через стенку в условиях нормы. При нарушении микрогемоциркуляции, что часто наблюдается при нарушении сосудистой П., эти методы могут быть малоинформативными, и тогда следует сочетать их с методами контроля состояния микрогемоциркуляции, напр. с помощью биомикроскопии или легкодиффундирующих индикаторов, гистогематический обмен которых не зависит от состояния сосудистой П. и тканевого метаболизма. Недостатком всех непрямых методов, основанных на регистрации накопления индикаторных веществ за пределами сосудистого русла, является необходимость учета массы факторов, способных существенно повлиять на уровень индикатора в изучаемом участке. Кроме того, эти методы довольно инерционны и не позволяют изучать кратковременные и обратимые изменения сосудистой П., особенно в сочетании с изменением микрогемоциркуляции. Эти трудности удается частично преодолеть с помощью метода меченых сосудов, основанного на определении проникновения в сосудистую стенку слабодиффундирующего индикатора, накапливающегося в стенке и окрашивающего ее. Окрашенные (меченые) участки выявляются с помощью светового микроскопа и являются доказательством нарушения П. эндотелия. В качестве индикатора может быть использован коллоидный уголь, образующий легко выявляемые темные скопления в местах грубого нарушения эндотелиального барьера. Изменения активности микровезикулярного транспорта этим методом не регистрируются и необходимо применять другие индикаторы, переносимые через эндотелий микровезикулами.
Возможности изучения нарушений сосудистой П. в условиях клиники более ограниченны, т. к. большинство методов, основанных на использовании микромолекулярных легко диффундирующих индикаторов (в т. ч. и радиоизотопов), не позволяют однозначно судить о состоянии барьерно-транспортной функции стенок кровеносных сосудов.
Сравнительно широко применяют метод, основанный на определении количественных различий в содержании белка в пробах артериальной и венозной крови, взятых одновременно (см. Лендиса проба). При вычислении процента потери белка кровью в процессе ее перехода из артериального русла в венозное необходимо знать процент потери воды, который определяется по разнице в гематокрите артериальной и венозной крови. В своих исследованиях на здоровых людях В. П. Казначеев и А. А. Дзизинский (1975) в качестве показателей нормальной П. сосудов верхней конечности вывели следующие величины: для воды в среднем 2,4-2,6%, для белка 4-4,5% , т. е. при прохождении по сосудистому руслу 100 мл крови в лимф. русло поступает ок. 2,5 мл воды и 0,15-0,16 г белка. Следовательно, за сутки в организме человека должно образовываться не менее 200 л лимфы, что в десятки раз превышает реальную величину суточной лимфопродукции в организме взрослого человека. Очевидно, что недостатком метода является допущение, согласно к-рому различия в гематокрите артериальной и венозной крови объясняются лишь изменением содержания в крови воды за счет ее выхода за пределы сосудистого русла.
В клин. практике о состоянии регионарной сосудистой П. нередко судят по наличию внутритканевых или полостных скоплений свободной жидкости, богатой белком. Однако при оценке состояния сосудистой П., напр. в брюшной полости, может быть сделано ошибочное заключение, поскольку обменные микрососуды этих органов и тканей в норме характеризуются высокой П. для макромолекул благодаря прерывистости или пористости их эндотелия. Увеличение фильтрационного давления в таких случаях ведет к образованию богатого белком выпота. Особенно проницаемы для белковых молекул венозные синусы и синусоиды.
Следует отметить, что повышенный выход плазменных белков в ткань и развитие тканевого отека (см.) не всегда сопутствуют повышению сосудистой П. Микрососуды (капилляры и венулы), эндотелий которых в норме слабопроницаем для макромолекул, приобретают эндотелиальные дефекты; через эти дефекты легко выходят в подэндотелиальное пространство введенные в кровоток индикаторы - макромолекулы и микрочастицы. Однако признаки тканевого отека при этом отсутствуют - так наз. безотековая форма нарушения сосудистой проницаемости. Подобное явление наблюдается, напр., в мышцах животных при развитии в них нейродистрофического процесса, связанного с перерезкой двигательного нерва. Сходные изменения в тканях человека описаны, напр., при старении и сахарном диабете, когда образуются так наз. ацеллюлярные капилляры, т. е. обменные микрососу ды с частично или полностью слущенными эндотелиальными клетками (признаки тканевого отека при этом также отсутствуют). Все эти факты говорят, с одной стороны, об относительности связи тканевых отеков с повышением сосудистой П., а с другой - о существовании внесосудистых механизмов, ответственных за распределение воды и веществ между кровью и тканями.
Факторы нарушения сосудистой проницаемости
Факторы нарушения сосудистой проницаемости условно делят на две группы: экзогенные и эндогенные. Экзогенные факторы нарушения сосудистой П. различной природы (физической, химической и др.) в свою очередь делятся на факторы, непосредственно влияющие на сосудистую стенку и ее барьерно-транспортную функцию напр., гистамин, введенный в сосудистое русло, различные токсины и т. п.), и факторы нарушения П. непрямого действия, эффект которых опосредуется через эндогенные факторы.
К уже известным эндогенным факторам нарушения сосудистой П. (гистамин, серотонин, кинины) стали относить большое число других, в частности простагландины (см.), причем последние не только повышают сосудистую П., но и усиливают действие других факторов; многие из эндогенных факторов продуцируются различными ферментными системами крови (системой фактора Хагемана, системой комплемента и др.).
Повышают сосудистую П. и иммунные комплексы. Из фактора, ответственного за «отсроченное» повышение сосудистой П. при развитии феномена Артюса, Йосинага (1966) выделил псевдоглобулин; Куроянаги (1974) открыл новый фактор П., обозначенный им как Ig-PF. По своим свойствам он существенно отличается от гистамина, кининов, анафилатоксина и калликреина, действует дольше, чем гистамин и брадикинин, угнетается витаминами K1 и K2.
Многие факторы нарушения сосудистой П. продуцируются лейкоцитами. Так, с поверхностью нейтрофилов связана протеаза, образующая из белков плазмы нейтральный пептидный медиатор, повышающий соудистую П. Белковый субстрат протеазы имеет мол. вес (массу) 90 000 и отличается от кининогена.
В лизосомах и специфических гранулах клеток крови содержатся катионные белки, способные нарушать сосудистую П. Их действие опосредуется гистамином тучных клеток.
Различные эндогенные факторы нарушения сосудистой П. действуют в тканях одновременно или последовательно, вызывая в. сосудистой П. фазовые сдвиги. В связи с этим выделяют ранние, отсроченные и позд ние изменения сосудистой П. Ранняя фаза - фаза действия гистамина (см.) и серотонина (см.). Вторая фаза развивается после периода мнимого благополучия, спустя 1-3 часа после первичного повреждения - замедленная, или отсроченная фаза; ее развитие обусловливается действием кининов (см.) или простагландинов. Развитие этих двух фаз зависит от уровня комплемента и угнетается антикомплементарной иммунной сывороткой. Через сутки после повреждения развивается третья фаза, связываемая с действием цито- и протеолитических ферментов, освобождающихся из лизосом лейкоцитов и лимфоцитов. В зависимости от природы первичного повреждающего агента количество фаз может быть разным. В раннюю фазу сосудистая П. нарушается гл. обр. на уровне венул, в последующие фазы процесс распространяется на капиллярное русло и артериолы.
Рецепция факторов проницаемости сосудистой стенкой. Эндогенные факторы нарушения П. представляют наиболее важную группу причин нарушения сосудистой П. Отдельные из них находятся в тканях в готовом виде (гистамин, серотонин) и под влиянием различных патогенных воздействий освобождаются из депо, в роли которых выступают тучные клетки и клетки крови (базофилы, тромбоциты). Другие факторы являются продуктом разных биохим. систем как в месте первичного повреждения, так и на расстоянии от него.
Вопросы происхождения факторов П. сами по себе важны для решения практических задач профилактики и лечения нарушений сосудистой П. Однако появление фактора П. еще не достаточно для нарушения сосудистой П. Для того чтобы фактор П. стал действительно фактором нарушения сосудистой П., он должен быть «замечен», т. е. рецептирован, сосудистой стенкой (если только он не обладает деструктурирующей способностью подобно цитолитическим агентам). Известно, напр., что гистамин, введенный в общий кровоток, нарушает сосудистую П. лишь в определенных органах и тканях, тогда как в других тканях (головной мозг, легочная ткань, эндоневрий и др.) он не эффективен. У лягушек введение в сосудистое русло серотонина и брадикинина вообще не вызывает нарушения сосудистой П. Однако причины неэффективности гистамина в обоих случаях различны.
По современным данным, эндотелий обменных микрососудов теплокровных животных и человека обладает чувствительностью к большому числу разнообразных агентов, т. е. характеризуется высокой рецепторной способностью. Что касается гистамина - одного из основных факторов П., вызывающего острое и значительное (хотя и кратковременное) нарушение сосудистой П., то экспериментальные данные говорят о наличии в эндотелии двух типов гистаминовых рецепторов H1 и H2, играющих разную роль в механизме действия гистамина. Именно стимуляция H1-рецепторов приводит к нарушению сосудистой П., характерному для действия гистамина.
При действии некоторых эндогенных факторов П., в частности гистамина, наблюдается тахифилаксия (см.) и повторное применение (через 30 мин.) агента уже не нарушает сосудистую П. Подобная временная нечувствительность эндотелия микро-сосудов не объясняется временной блокадой соответствующих рецепторов, хотя в некоторых случаях это и может быть. В случае с гистамином механизм тахифилаксии, по нек-рым сведениям, имеет внерецепторную локализацию. Это доказывается, в частности, фактом развития перекрестной тахифилаксии, когда применение гистамина ведет к развитию устойчивости эндотелия не только к самому гистамину, но и к солям лантана, действующим в обход рецепторов. Возникновение перекрестной тахифилаксии может быть одной из причин неэффективности отдельных факторов П., действующих одновременно или последовательно.
Ультраструктурные основы и эффекторные механизмы нарушения сосудистой проницаемости
Рис. 2. Пути и механизмы транскапиллярного обмена веществ в условиях нормы (а) и патологии (б): 1 - трансцеллюлярная диффузия; 2 - диффузия и ультрафильтрация в области плотных межклеточных соединений; 3 - диффузия и ультрафильтрация в области простых межклеточных соединений; 4 - микровезикулярный транспорт в обход плотных межклеточных соединений; 3а и 4а - патологические межклеточные каналы типа «гистаминовых щелей»; 5 - микровезикулярный транспорт; 6 - образование трансцеллюлярного канала путем слияния микровезикул; 7 - фагоцитарные вакуоли в перицитах; 8 - микрочастицы индикатора сосудистой проницаемости (БМ - базальная мембрана, ЭН1, ЭН2, ЭН3 - эндотелиоциты, ПЦ - перициты).
Электронно-микроскопическими исследованиями выявлено, что морфол. основой повышения сосудистой П. является образование широких каналов в области межклеточных соединений в эндотелии (рис. 2). Такие каналы, или «течи», часто называют гистаминовыми щелями, т. к. их образование типично для действия на сосудистую стенку гистамина и впервые подробно изучено именно при его действии. Гистаминовые щели образуются гл. обр. в стенках венул тех органов и тканей, где отсутствуют малопроницаемые гистогематические барьеры типа гематоэнцефалического и др. Локальные расхождения межклеточных контактов обнаружены при нейрорегуляторных расстройствах, механических, термических, химических и других видах повреждений тканей, при действии различных биорегуляторов (серотонина, брадикинина, простагландинов Е1 и Е2 и т. д.). Нарушение межклеточных контактов возникает, хотя и с большим трудом, в капиллярах и артериолах и даже в более крупных сосудах. Легкость образования гистаминовых щелей прямо пропорциональна исходной структурной слабости межклеточных соединений, к-рая возрастает при переходе от артериол к капиллярам и от капилляров к венулам, достигая максимума на уровне посткапиллярных (перицитарных) венул.
Неэффективность гистамина в нарушении сосудистой П. некоторых органов хорошо объясняется именно с точки зрения развития плотных соединений в эндотелии микрососудов этих органов, напр. мозга.
В теоретическом и практическом отношении важен вопрос об эффекторных механизмах, лежащих в основе образования структурных дефектов типа гистаминовых щелей. Эти ультраструктурные сдвиги типичны именно для начальной фазы острого воспаления (см.), когда, по данным И. И. Мечникова (1891), повышение сосудистой П. биологически целесообразно, т. к. благодаря этому обеспечивается повышенный выход фагоцитов к очагу повреждения. Можно добавить, что повышенный выход плазмы в таких случаях также целесообразен, т. к. при этом в очаг доставляются антитела и средства неспецифической защиты. Т. о., повышение сосудистой П. в очаге воспаления можно рассматривать как специфическое состояние барьерно-транспортной функции стенок микро-сосудов, адекватное новым условиям существования ткани, а изменение сосудистой П. при воспалении и сходных ситуациях - не как нарушение, а как новое функциональное состояние, способствующее восстановлению нарушенного тканевого гомеостаза. Следует учитывать, что в некоторых органах (печень, селезенка, костный мозг), где в соответствии с особенностями органных функций существует непрерывный обменный поток клеток и макромолекул, межклеточные «течи» являются нормальными и постоянными образованиями, представляющими собой утрированные гистаминовые щели, но в отличие от истинных гистаминовых щелей способны к длительному существованию. Истинные гистаминовые щели образуются в первые же секунды после воздействия на эндотелий медиаторов острого воспаления и в большинстве своем через 10-15 мин. закрываются. Механизм образования гистаминовых щелей имеет защитный, филогенетически обусловленный характер и связан со стереотипной реакцией на клеточном уровне, запускаемой стимуляцией разных типов рецепторов.
Природа этой стереотипной реакции долго оставалась неизученной. И. И. Мечников считал, что повышение сосудистой П. при воспалении связано с сокращением эндотелиальных клеток. Однако позже было установлено, что эндотелиоциты в сосудах теплокровных не относятся к категории клеток, активно меняющих свою форму подобно мышечным. Роули (D. A. Rowley, 1964) высказал предположение, что расхождение эндотелиоцитов является следствием повышения внутрисосудистого давления и связанного с этим перерастяжения эндотелия. Прямые измерения доказали неприемлемость этой гипотезы в отношении венул и капилляров, однако для артериальных сосудов она имеет определенную ценность, т. к. при нарушении тонической активности мышечной оболочки высокое внутрисосудистое давление действительно способно вызвать перерастяжение эндотелия и повреждение межклеточных контактов. Но и в этом случае появление гистаминовых щелей в интиме не всегда связано с действием трансмурального давления. Робертсон и Кайраллах (A. L. Robertson, P. A. Khairallah, 1972) в опытах на изолированном сегменте брюшной аорты кролика показали, что широкие щели в эндотелии образуются под влиянием ангиотензина II в местах округления и укорочения эндотелиоцитов. Сходные морфол. сдвиги обнаружены и в эндотелии обменных микрососудов кожи при местном применении ангиотензина II, простагландина Е1 и сывороточных триглицеридов.
О. В. Алексеев и А. М. Чернух (1977) обнаружили у эндотелиоцитов обменных микрососудов способность, к быстрому увеличению содержания в цитоплазме микрофибриллярных структур, сходных по своим морфол. признакам с актиновыми микронитями. Этот обратимый феномен (так наз. феномен оперативной структурализации микрофибриллярного аппарата) развивается под влиянием факторов, вызывающих образование широких межклеточных щелей. Обратимость феномена в случае применения гистамина затрудняет его выявление и хорошо объясняет кратковременность и обратимость существования гистаминовых щелей. С помощью цитохалазина-Б, блокирующего образование актиновых микро-фибрилл, выявляется патогенетическое значение данного феномена в механизме образования межклеточных гистаминовых щелей. Эти факты говорят о наличии у эндотелиоцитов скрытой способности к сокращению, реализующейся в условиях, когда прежний уровень сосудистой П. оказывается неадекватным и требуется сравнительно быстрое и обратимое его изменение. Изменение сосудистой П. выступает, т. о., как особый акт биол. регуляции, обеспечивающий адаптацию барьерно-транспортной функции сосудистого эндотелия в соответствии с новыми местными потребностями, остро возникшими в связи с изменением условий жизнедеятельности ткани.
Наличие в тканях механизма изменения сосудистой П. можно отнести к так наз. факторам риска, т. к. срабатывание этого механизма в неадекватных условиях может стать причиной нарушения тканевого гомеостаза и органной функции, а не проявлением действия адаптационно-защитных механизмов. Основные пути нарушения сосудистой П. представлены на схеме. В основе изменения сосудистой П. лежат механизмы, не только приводящие к образованию межклеточных каналов (гистаминовых щелей), но и влияющие на активность клеточной поверхности (т. е. на микровезикуляцию и микровезикулярный транспорт, вакуолизацию и микропузыреобразование). Результатом может быть перфорация эндотелиоцитов с образованием более или менее обширных и долговременных трансцеллюлярных каналов.
Большое значение в механизмах нарушения сосудистой П. придается локальным изменениям поверхностного электрического заряда, особенно на мембранах, закрывающих поры в фенестрированных капиллярах (напр., почечных клубочков). По нек-рым данным, одно только изменение заряда может быть основой повышения выхода белков из клубочковых капилляров. Т. о. доказывается ограниченность теории пор, в соответствии с к-рой П. зависит лишь от размера и соотношения гипотетических крупных и мелких пор в стенках сосудов. В условиях патологии эффект повышения пористости эндотелия может достигаться разными путями: образованием межклеточных каналов типа гистаминовых щелей; усилением микровезикулярного и интравакуолярного транспорта; перфорацией эндотелиоцитов на основе усиления микровезикуляции, вакуолизации или микропузыреоб разования в эндотелии; микроочаговой деструкцией эндотелиоцитов; слущиванием эндотелиоцитов; изменением физ.-хим. свойств поверхности эндотелиоцитов и др. (см. Микроциркуляция ]]). Этот же эффект может быть достигнут и за счет внестеночных механизмов, в частности за счет изменения связывательной способности макромолекул крови, с к-рыми взаимодействуют почти все известные индикаторы, используемые для оценки состояния сосудистой П. В условиях патологии чаще всего одновременно или последовательно действуют разные из перечисленных механизмов. Так, напр., гистамин повышает пористость сосудистой стенки за счет образования гистаминовых щелей в эндотелии венул, а также путем влияния на поверхность эндотелиоцитов и связанные с ее активностью транспортные процессы и ультраструктурные трансформации (образование трансцеллюлярных пор, фенестр, микроканальцев и др.). Необходимо учитывать, что при этом часто меняется толщина эндотелиоцитов и глубина межклеточных щелей, что может оказывать существенное влияние на проницаемость сосудистой стенки как диффузионного барьера. Совершенно не изучен вопрос о поведении в условиях патологии биохим. механизмов, препятствующих или, наоборот, способствующих проникновению через сосудистую стенку веществ, особенно биологически активных. Известно, напр., что эндотелиоциты мозговых капилляров в норме обладают ферментативной активностью, разрушающей серотонин и тем самым препятствующей его проникновению как из крови в мозг, так и в обратном направлении. Эндотелий легочных капилляров содержит кининазу II, локализуемую в микропиноцитозных везикулах и обеспечивающую разрушение брадикинина и одновременно превращение ангиотензина I в ангиотензин II (гипертензии). Т. о., эндотелий осуществляет своеобразный контроль баланса гуморальных биорегуляторов, активно влияет на гистогематический обмен этих агентов.
Направленное вмешательство осуществляется на трех уровнях (см. схему). Первый уровень - воздействие на процесс образования причинных (рецептируемых) факторов - практически не используется, хотя имеются отдельные медикаментозные средства, способные действовать именно на этом уровне. Напр., резерпин влияет на депонирование факторов нарушения П. в тучных клетках, представляющих собой основной источник медиаторов острого воспаления (гистамина и серотонина); антипростагландиновые средства угнетают синтез простагландинов - ацетилсалициловая кислота и др.
Второй уровень является основным в практике разработки средств профилактики и лечения нарушений сосудистой П. Он соответствует процессу рецепции причинного фактора. Используется значительное число антигистаминовых, антисеротониновых и антибрадикининовых препаратов, предупреждающих нарушения сосудистой П., вызываемые соответствующими медиаторами. Достоинством и в то же время недостатком данных препаратов, действующих путем блокады специфических рецепторов, является их высокая специфичность. Такая специфичность делает их неэффективными в условиях множественности этиол. факторов, действующих одновременно или последовательно, что обычно наблюдается в клин. практике. Важно и то, что исключение действия одного фактора или нескольких, определяющих развитие одной фазы нарушения сосудистой П., не исключает развитие последующих фаз. Эти недостатки могут быть преодолены путем вмешательства на третьем уровне.
Третий уровень - воздействие на внутриклеточные (субклеточные) эффекторные механизмы, через которые непосредственно реализуется действие факторов П., причем единые для действия различных патогенных агентов. Реальность и эффективность такого подхода удается продемонстрировать в эксперименте путем применения вещества (цитохалазина-Б), угнетающего феномен оперативной структурализации микрофибриллярного аппарата в эндотелиоцитах (образование актинового геля и актиновых микрофибрилл).
В клин. практике с целью нормализации повышенной сосудистой П. используют витамин Р (см. Биофлавоноиды) и соли кальция. Однако эти препараты не могут рассматриваться как специфические леч. средства при нарушении сосудистой П., хотя они и оказывают общеукрепляющее влияние на гистогематические барьеры, мембраны и стенку сосудов в частности.
Для повышения сосудистой П. могут быть использованы различные эндогенные факторы П., напр. гистамин, или вещества, освобождающие их из тканевых депо.
Библиография: Алексеев О. В. Микроциркуляторный гомеостаз, в кн.: Гомеостаз, под ред. П. Д. Горизонтова, с. 278, М., 1976; Антонов В. Ф. Липиды и ионная проницаемость мембран, М., 1982; Биологические мембраны, под ред. Д. С. Парсонса, пер. с англ., М., 1978; Д е Робер тис Э., Новинский В. и С а э с Ф. Биология клетки, пер. с англ., М., 1967; Живая клетка, пер. с англ., под ред. Г. М. Франка, с. 130, М., 1962; К а з-начеевВ.П. и Д з и з и н с к и й А. А. Клиническая патология транскапиллярного обмена, М., 1975; Лайт фут Э. Явления переноса в живых системах, пер. с англ., М., 1977; Л а к ш м ин а р а я н а й а х Н. Мембранные электроды, пер. с англ., Л., 1979; Лев А. А. Моделирование ионной избирательности клеточных мембран, Л., 1976; Овчинников Ю. А., Иванов В. Т. и III к р о б А. М. Мембранно-активные комплексоны, М., 1974; Структура и функция клетки, пер. с англ., под ред. Г. М. Франка, с. 173, М., 1964; Трошин А. С. Проблема клеточной проницаемости, М. - Л., 1956; Чернух А. М., Александров П. Н. и Алексеев О. В. Микроциркуляция, М., 1975; Di Rosa М., Giroud J. Р. а. W 1 1-loughby D. A. Studies of the media-tors of the acute inflammatory response induced ln rats in different sites by carra-geenan and turpentine, J. Path., v. 104, p. 15, 1971; M a j n о G. а. P а 1 a-de G. E. Studies on inflammation, I. The effect of histamine and serotonin on vascu-lar permeability, an electron microscopic study, J. biophys. biochem. Cytol., v. 11, p. 571, 1961; M a j n о G., S h e a S. M. a. Leventhal M. Endothelial cont-raction induced by histamine-type medi-ators, J. Cell Biol., v. 42, p. 647, 1969: Shimamoto T. Contraction of endothelial cells as a key mechanism in athero-genesis and treatment of atherosclerosis with endothelial cell relaxants, в кн.: Atherosclerosis III, ed. by G. Schettler a. A. Weizel, p. 64, В.-N. Y., 1974.
B. Ф. Антонов; О. В. Алексеев (пат. физ.).
Мембранные методы очистки основаны на различной проницаемости мембран для компонентов очищаемой газовой смеси.[ ...]
Селективную проницаемость мембран в процессе ультрафильтрации объясняет чисто ситовой механизм разделения - частицы примесей, имеющие больший размер, чем размеры пор мембраны, через мембрану не проходят, через нее профильтровывается только вода.[ ...]
Селективность и проницаемость мембран должны рассматриваться во взаимосвязи с затратами на получение воздуха, обогащенного кислородом. Расходы на разделение воздуха зависят от проницаемости, селективности, геометрических параметров мембран, производительности модуля, стоимости электроэнергии и других факторов. Стоимость обогащенного кислородом воздуха оценивается по отношению к эквивалентно чистому кислороду, определяемому как количество чистого кислорода, необходимого для смешения с воздухом (21% кислорода) при получении того же количества и процентного содержания кислорода, которое получается в рассматриваемом газоразделительном процессе.[ ...]
Ультрафильтрация - мембранный процесс разделения растворов, осмотическое давление которых мало. Этот метод используется при отделении сравнительно высокомолекулярных веществ, взвешенных частиц, коллоидов. Ультрафильтрация по сравнению с обратным осмосом - более высокопроизводительный процесс, так как высокая проницаемость мембран достигается при давлении 0,2-1 МПа.[ ...]
Промывка твердых отходов 434, 425 Проницаемость мембран 273 Процеживание 197 сл.[ ...]
Ионы кальция оказывают большое влияние на мембранные структуры. На необходимость ионов Са2+ для стабилизации мембран указывалось достаточно давно. Было показано, что для образования поверхностной мембраны на эндоплазматической капле, изолированной из интерно-дальных клеток харовых водорослей, необходимо присутствие в окружающем растворе ионов Са2+. Присутствие Са2+ в концентрации 10 4 М способствовало образованию поверхностной мембраны на капле, хотя и недостаточно прочной; более прочная мембрана образовывалась при концентрации 10"3 М и особенно 10 2 М. При удалении ионов кальция (например, при обработке хелатами или при отсутствии Са2+ в среде) отмечается ослизнение корневых волосков, а также повышается проницаемость мембран к другим веществам. Ионы Са2+ изменяют и электрические свойства как искусственных, так и естественных мембран, умень-шая плотность заряда на мембранной поверхности. Недостаток Са приводит к возрастанию вакуолизации, изменению хромосом, разрыву мембран ЭПР и других внутриклеточных компартментов.[ ...]
С ростом концентрации разделяемого раствора проницаемость мембран уменьшается, с ростом давления - увеличивается. После процесса очистки получается фильтрат, обедненный на 90-99,5 °/о исходными соединениями, и концентрат, направляемый на дальнейшую переработку.[ ...]
Реакция на ацетилхолин и биогенные амины состоит в изменении проницаемости мембран к ионам и/или индукции синтеза вторичных посредников. Присутствие в растительной клетке и ее органеллах цАМФ, цГМФ, Са2+, а также ферментов синтеза и катаболизма подтверждает возможность локальной медиации.[ ...]
Так, под действием СВЧ ЭМИ (2,45 ГГц) обнаружено увеличение катионной проницаемости мембран эритроцитов при комнатной температуре, в то время как в отсутствие СВЧ ЭМИ подобный эффект наблюдается только при температуре 37 °С.[ ...]
Фонды метаболитов не равномерно распределены по клетке, а разделены мембранами и локализованы в отдельных отсеках (камерах, компартментах). Компартменты метаболических фондов клетки связаны между собой транспортными потоками. В соответствии с избирательной проницаемостью мембран происходит пространственное перераспределение интермедиатов и продуктов обмена. Например, в клетке запас АТФ поддерживается за счет "горизонтальных" связей процессов фотосинтетического и окислительного фосфоршшрования.[ ...]
Концентрация раствора. С ростом концентрации разделяемого раствора проницаемость мембран уменьшается вследствие увеличения осмотического давления растворителя и влияния концентрационной поляризации. При значении критерия Рейнольдса 2000-3000 концентрационная поляризация практически отсутствует, однако турбулизация раствора связана с его многократной рециркуляцией, т. е. с затратами энергии, и приводит к накоплению взвешенг ных частиц в растворе и появлению биологических обрастаний.[ ...]
Понижение температуры воды, ведущее к охлаждению рыб, ведет и к увеличению проницаемости мембран, которые теряют способность поддерживать ионные градиенты. При этом нарушается сопряженность ферментативных реакций, перестают работать ионные насосы, нарушается работа центральной и периферической нервной системы, угнетается работа кардиореспираторного аппарата, что в конечном счете может привести к развитию гипоксии. При перегреве или охлаждении рыб, возникающих в результате резкого изменения температуры в ограниченное время, определенная роль принадлежит осмотическим стрессам вследствие нарушения способности организма поддерживать определенную концентрацию ионов и белков в крови . Так, например, снижение температуры с 25 до 11°С вызывает у тиляпии, содержавшейся в пресной воде, развитие коматозного состояния, сопровождающегося снижением концентрации ионов натрия и хлора и общего белка крови . По мнению авторов, гибель рыб наступает из-за развития осморегуляторного коллапса и угнетения функции почёк. Косвенным подтверждением этого предположения может служить предотвращение температурной комы у рыб, содержащихся в разбавленной морской воде, что согласуется с более ранними наблюдениями повышения терморезистентности рыб вследствие добавления в воду ионов натрия, кальция и магния . Следует, однако, иметь в виду, что причины гибели рыб при повышенных или пониженных температурах различны и зависят от продолжительности и интенсивности температурного воздействия.[ ...]
Величина pH. Изменение первоначального значения pH обычно приводит к понижению проницаемости мембран . Влияние pH на селективность мембран невелико. Летучие кислоты плохо задерживаются мембранами, поэтому предварительная нейтрализация летучих кислот повышает селективность процесса разделения.[ ...]
При высоких концентрациях солей в трехкамерном электродиализаторе с инертными мембранами максимальный выход по току не превышает 20%.[ ...]
Получены положительные результаты очистки сточных вод от ОП-7 обратным осмосом при давлении 5 МПа. Проницаемость мембран составляла 5-20,8 л/(м2-ч) при концентрации ОП-7 в фильтрате 1-18 мг/л .[ ...]
ПАВ (алкилсульфаты) стимулируют размножение бактерий в наибольшей степени. Кроме того, ПАВ, изменяя проницаемость мембран живых клеток (С. С. Строев, 1965 и др.), возможно, способствуют лучшей усвояемости микробами пищевых веществ, содержащихся в воде.[ ...]
Природа растворенного вещества оказывает определенное влияние на селективность и в меньшей степени на проницаемость мембран. Это влияние заключается в том, что неорганические вещества задерживаются мембранами лучше, чем органические с той же молекулярной массой; среди родственных соединений, например, гомологов, лучше задерживаются вещества с большей молекулярной массой; вещества, образующие связи с мембраной, например, водородную, задерживаются мембраной тем лучше, чем менее прочна эта связь; селективность задержания высокомолекулярных соединений ультрафильтрацией тем больше, чем больше молекулярная масса растворенного вещества.[ ...]
Мембраны из ацетата целлюлозы могут работать в интервале pH 4,5-7, а из химически стойких полимеров - при pH 1 -14. Проницаемость мембран выбирается такой, чтобы обеспечивать проход воды, растворимых солей и задерживать масла. Размер пор в мембранах обычно составляет в пределах 2,5-10 нм. Установка оборудована вспомогательными трубопроводами для промывки мембран фильтратом или деминерализованной водой, снабжена контрольно-измерительными приборами и автоматическими устройствами.[ ...]
При значительном снижении внутриклеточной разности потенциалов до определенного порогового уровня наблюдается резкое изменение проницаемости мембран и обращение (реверсия) ионных потоков. Ионы кальция из наружной среды, окружающей клетку, поступают в нее, а ионы хлора и ионы калия выходят из клетки в омывающий раствор.[ ...]
Толерантность связана с внутренними факторами и включает такие метаболические процессы, как селективное поглощение ионов, пониженная проницаемость мембран, иммобилизация ионов в отдельных частях растений, удаление ионов из метаболических процессов с помощью образования запаса в нерастворимых формах в различных органах, адаптацию к замещению физиологического элемента токсичным в энзиме, удаление ионов из растений при вымывании через листья, соковыделении, сбрасывании листьев, выделении через корни. Толерантные растения могут стимулироваться при повышенных концентрациях металлов, что свидетельствует об их физиологической потребности в избытке. Отдельные виды растений способны-накапливать значительное количество тяжелых металлов без видимых признаков угнетения. Другие растения не имеют такой способности (см. табл.[ ...]
Давление является одним из основных факторов, определяющих производительность установок обратного осмоса. Производительность мембран увеличивается с повышением избыточного давления. Однако, начиная с некоторого давления, проницаемость мембран снижается вследствие уплотнения полимерного материала мембраны.[ ...]
Установлено также, что низкие ([ ...]
Поскольку полисахариды гемицеллюлоз имеют среднечисловой молекулярный вес не выше 30 000, применение обычной осмометрии затруднено вследствие проницаемости мембран для низкомолекулярных фракций. Предложенный Хиллом метод осмометрии в паровой фазе имеет ряд преимуществ перед другими методами. Этот метод основан на измерении разности давления паров раствора и растворителя и заключается в следующем . Каплю раствора и каплю растворителя помещают на два спая термопары и выдерживают в атмосфере, насыщенной парами чистого растворителя. Вследствие пониженного давления пара раствора часть пара сконденсируется на капле раствора, повышая температуру капли и термопары. Возникающая электродвижущая сила измеряется гальванометром. Верхний предел измеряемой величины молекулярного веса около 20 000, точность измерения 1 %.[ ...]
Наконец, мембраны эндоплазматического ретикулума - это те поверхности, по которым распространяются биотоки, являющиеся сигналами, меняющими избирательную проницаемость мембран и тем самым активность ферментов. Благодаря этому одни химические реакции пускаются в ход, другие тормозятся - обмен веществ подчиняется регуляции и протекает координированно.[ ...]
Нлазмалемма регулирует вход веществ в клетку и выход их из нее, обеспечивает избирательное проникновение веществ в клетку и из клетки. Скорость проннкновепия сквозь мембрану разных веществ различна. Хорошо проникают через нее вода и газообразные вещества. Легко проникают также жирорастворимые вещества,- вероятно, благодаря тому, что она имеет липидный слой. Предполагается, что липидный слой мембраны пронизан порами. Это позволяет проникать сквозь мембрану веществам, нерастворимым в жирах. Поры несут электрический заряд, поэтому проникновение через них ионов не вполне свободно. При некоторых условиях заряд пор меняется, и этим регулируется проницаемость мембран для ионов. Однако мембрана неодинаково проницаема и для разных ионов с одинаковым зарядом, и для разпых незаряжепных молекул близких размеров. В этом проявляется важнейшее свойство мембраны - избирательность ее проницаемости: для одних молекул и ионов она про-пицаема лучше, для других хуже.[ ...]
В настоящее время общепризнанным является механизм действия медиаторов в животных и растительных клетках, который основывается на регуляции ионных потоков. Изменения мембранных потенциалов обусловлены сдвигами ионной проницаемости мембран путем открытия или закрытия ионных каналов. С этим явлением и связаны механизмы возникновения и распространения ПД в животных и растительных клетках. В животных клетках - это №7К+-каналы, контролируемые ацетил-холином, и Са2+-каналы, чаще зависимые от биогенных аминов. В растительных клетках возникновение и распространение ПД связывается с кальциевыми, калиевыми и хлорными каналами.[ ...]
С большей воспроизводимостью и устойчивостью стабильный поток газов и паров может быть получен способами, основанными на диффузии газов или паров жидкости через капилляр (рис. 10) или проницаемую мембрану (рис. 11) в поток газа-разбавителя. В таких методах наблюдается равновесие между газовой фазой и адсорбирующими поверхностями аппаратуры, что обеспечивает стабильность микропотока.[ ...]
Увеличение температуры приводит к уменьшению вязкости и плотности раствора и одновременно к возрастанию его осмотического давления. Уменьшение вязкости и плотности раствора усиливает проницаемость мембран, а увеличение осмотического давления снижает движущую силу процесса и уменьшает проницаемость.[ ...]
В любой живой системе существует РЭП, и было бы удивительно, если бы не было. Это означало бы абсолютное равенство концентраций электролита во всех клетках, органах, наружных растворах либо полное совпадение величин проницаемости мембран ко всем катионам и анионам.[ ...]
В опыте 6, аналогичном опыту 1, определяли количество выделившегося калия и воднорастворимого органического вещества при разных концентрациях атразина. Судя по полученным результатам, можно сказать, что атразин не увеличивает проницаемость мембран для низкомолекулярных органических веществ и увеличивает для калия. Этот эффект был пропорционален концентрации атразина.[ ...]
При обследовании лиц, подвергавшихся во время работы действию радиации малого уровня (например, радиологи и техники, работающие с рентгеновским излучением, дозы которого измерялись индивидуальными дозиметрами) с помощью метода меченых атомов , проводились анализы крови на проницаемость мембран эритроцитов при прохождении одновалентных катионов. Было обнаружено, что проницаемость мембран эритроцитов у лиц, подвергавшихся облучению, значительно выше, чем у тех, кто не облучался. Кроме того, график зависимости позволил установить быстрое возрастание проницаемости при малом облучении; при больших дозах кривая становится пологой, аналогично наблюдению Стокке при изучении животных (см. рис. Х1У-3). Эти данные согласуются с результатами, полученными Петкау .[ ...]
При обессоливании минерализованных сточных вод гиперфильтрацией через полупроницаемые мембраны основные параметры - концентрацию растворенных веществ в концентрате и фильтрате необходимо определять на единицу ширины мембраны при заданной ее длине, разделяющей способности, коэффициенте проницаемости мембран, давлении, расходах исходной воды, фильтрата и концентрата.[ ...]
Возможность подобной адаптации обусловлена зависимостью термодинамических, .химических, кинетических констант от температуры. Эта зависимость, в общем, определяет направление и скорость химических реакций, конформационных переходов биологических маодомолекул,фазовых переходов липидов, изменение проницаемости мембран и других процессов, функционирование которых обеспечивает жизнедеятельность организмов при повышенной температуре.[ ...]
Все это пока лишь первые шаги в области применения омагниченной воды в медицине. Однако уже имеющиеся сведения свидетельствуют о перспективности применения омагничивания водных систем в этой области. Ряд медицинских проявлений возможно (гипотетически) связан с тем, что омагничивание водных систем повышает проницаемость мембран.[ ...]
Установлено, что полимерные пленки, выпускаемые промышленностью для ультрафильтрации, ионного обмена , а также мембраны из коллодия, желатины, целлюлозы и других материалов , имеют хорошую селективность, но малую проницаемость (0,4 л/м ч при давлении 40 am). Мембраны, приготовляемые по специальной прописи из смеси ацетатцеллюлозы, ацетона, воды, перхлората магния и соляной кислоты (соответственно 22,2; 66,7; 10,0; 1,1 и 0,1 весовых процента), позволяют опреснять воду с 5,25 до 0,05% NaCl и имеют проницаемость 8,5-18,7 л!м2 ■ ч при рабочем давлении 100-140 am , срок их службы не менее 6 месяцев . Электронно-микроскопические исследования этих мембран , так как, по предварительным расчетам 1192], обратный осмос может стать конкурентноспособным с другими способами опреснения воды при повышении проницаемости мембран до 5 м31мг в сутки.[ ...]
Потенциал покоя клеточной стенки. Клеточная стенка (оболочка) имеет отрицательный поверхностный заряд. Наличие этого заряда придает клеточной стенке отчетливо выраженные катионообменные свойства. Клеточная стенка характеризуется преимущественной избирательностью к ионам Са2+, который играет важную роль в регуляции проницаемости мембран по отношению к ионам К и №+.[ ...]
Таким образом, отмеченные эффекты указывают на то, что в культуральной жидкости микромицета Fusarium oxysporum помимо фузариевой кислоты содержатся и иные компоненты, обладающие высокой биологической активностью. Оценку степени патогенности различных изолятов фитопатогенных грибов можно производить на основе определения изменения проницаемости мембран растительных клеток к аммиаку.[ ...]
В результате снижается или прекращается новообразование АТФ, что ведет к подавлению процессов, зависящих от энергии дыхания. Нарушается также структура и избирательная проницаемость мембран, для поддержания которой необходима затрата энергии дыхания. Эти изменения приводят к снижению способности клеток поглощать и удерживать воду.[ ...]
С другой стороны, стабилизация пространственной структуры белка и других биополимеров осуществляется в значительной мере за счет взаимодействия: биополимер - вода. Основой функционирования живых систем считается водно-белково-нуклеиновый комплекс, поскольку только при наличии этих трех составляющих возможна нормальная жизнедеятельность мембран. Избирательная проницаемость мембран зависит от состояния воды. Экстраполируя кластерную модель воды на биологические системы, можно показать, что при разрушении кластера на определенны участках мембраны открывается путь для предпочтительного транспорта. Бесструктурная вода, например, препятствует повеДе нию протонов вблизи мембраны, тогда как по структурированно му каркасу протоны распространяются быстро.[ ...]
Описана схема непрерывного анализа газа с использованием ионоселективного электрода, которая может быть применена для определения содержания в газах НгЗ, НСЫ и НР. В обзоре работ НБС США среди других методов аттестации эталонных газов (смесей) указан также метод аттестации с помощью ионоселективных электродов для газов НСИ и НР. Из всех конструкций ионоселективных электродов обычно используют следующую: ионоселективная мембрана разделяет два раствора - внутренний и внешний (исследуемый). Для электрического контакта во внутренний раствор помещен вспомогательный электрод, обратимый к ионам внутреннего раствора, активность которых постоянна, вследствие чего постоянен и потенциал. На внутренней и внешней поверхностях мембраны возникает разность потенциалов, зависящая от разности активности ионов во внешнем и внутреннем растворах. Теория возникновения мембранного потенциала изложена в работе . В основном возникновение потенциала объясняется проницаемостью мембран либо только для катионов (катионоселективные), либо только для анионов (анионоселективные).
ПРОНИЦАЕМОСТЬ И ТРАНСПОРТ ВЕЩЕСТВ В БИОЛОГИЧЕСКИХ МЕМБРАНАХ
Проницаемость биологических мембран
Одна из важнейших функций биологической мембраны заключается в обеспечении обмена ионов и молекул между клеткой и окружающей средой. Способность биологических мембран пропускать через себя различные вещества называется проницаемостью . Изучение проницаемости клеток имеет большое значение, поскольку с данной функцией связаны практически все процессы жизнедеятельности клетки: метаболизм, генерация и проведение биопотенциалов, секреция, рецепция и т. д.
Транспорт веществ
Любая клетка очень точно поддерживает свой химический, в том числе и ионный состав. Постоянство ионного состава называется ионным гомеостазом и поддерживается за счёт транспорта веществ.
Транспорт веществ в организме можно разделить на три категории:
Дальний транспорт – перенос веществ между органами, его протяжённость в растениях может достигать нескольких десятков метров;
Ближний транспорт – перенос между соседними клетками;
Мембранный транспорт – перенос веществ через мембрану.
По энергетическим затратам мембранный транспорт можно разделить на 2 важнейших класса: активный и пассивный.
Пассивный транспорт не связан прямо с затратой химической энергии; он осуществляется в результате диффузии веществ в сторону меньшего электрохимического потенциала (где концентрация веществ и заряд меньше). Активный транспорт происходит при затрате химической энергии АТФ или переносе электрона по дыхательной цепи.
Виды пассивного транспорта веществ в клетках и тканях: диффузия, осмос.
Диффузия - основной механизм пассивного транспорта веществ, обусловленный наличием концентрационного градиента. Различают несколько видов диффузии:
1) простая диффузия, диффундирующее вещество движется по градиенту через мембрану, не образуя комплекса или проникая через канал;
2) облегченная диффузия , осуществляемая с помощью переносчиков - белков или молекулярных комплексов.
Простая диффузия- это самопроизвольный физический процесс проникновения вещества из области высокой в область меньшей его концентрации в результате теплового хаотического (броуновского) движения молекул.
С помощью простой диффузии через мембрану переносятся растворимые в липидах вещества, в частности такие хорошо растворимые в липидах и важнейшие для метаболического обмена вещества как кислород и углекислый газ. Через липидную фазу мембран в клетку могут проникать также яды и лекарства.
Математическое обоснование процесса диффузии впервые дал А. Фик. Согласно первому закону Фика поток вещества (J) прямо пропорционален градиенту концентрации dC/dx:
https://pandia.ru/text/78/170/images/image002_95.gif" width="433" height="56">
Учитывая это, формулу для потока вещества через мембрану можно записать в следующем виде:
https://pandia.ru/text/78/170/images/image004_68.gif" width="128" height="56">
Коэффициент проницаемости Р имеет размерность см/с и является количественной характеристикой способности конкретного вещества проникать через мембрану. Он аналогичен
коэффициенту диффузии (D), но зависит не только от природы вещества и температуры, но и от свойств мембраны.
DIV_ADBLOCK54">
Проникновение в клетку глюкозы, глицерина, аминокислот и некоторых других веществ не имеет линейной зависимости от их концентрации. Причем при определенных концентрациях скорость их проникновения значительно выше, чем при простой диффузии. Эта особенность объясняется тем, что в данном случае наблюдается не простая, а облегченная диффузия. Вещество самостоятельно диффундирует через мембрану, но скорость диффузии намного возрастает, если молекулы этого вещества образуют комплекс с молекулами переносчика, который хорошо растворяется в липидах. Молекулы-переносчики могут быть как подвижными, так и фиксированными в мембране - каналы .
Диффузия с участием переносчика, как и простая, происходит до тех пор, пока концентрация по обе стороны мембраны не станет одинаковой.
Разновидностью облегченной диффузии является так называемая обменная диффузия , при которой переносчик образует соединении с диффундирующим веществом и перемещается с ним от одной поверхности мембраны к другой, где молекула переносчика освобождается, ее место занимает другая молекула того же вещества и комплекс переносится обратно. При работе переносчиков в случае обменной диффузии концентрация веществ по обе стороны мембраны не изменяется. Существование обменной диффузии было доказано методом меченых атомов на эритроцитах, митохондриях и др.
Проникновение растворенных частиц, обладающих электрическим зарядом, через клеточную мембрану осуществляется по электрохимическому градиенту , а не по концентрационному.
Электрохимический потенциал – энергия, которую надо затратить для перемещения одного моля вещества из бесконечно удалённой точки пространства в данную точку с конкретными условиями.
Величина электрохимического потенциала описывается формулой:
где: - стандартный член;
Активность j-го иона
Химическая работа;
Парциальный моляльный обьем;
Механическая работа (работа по расширению объёиа)
Заряд иона;
Электрический потенциал;
Число Фарадея;
Электрическая работа.
Молекулы вещества всегда двигаются в сторону своего более низкого электрохимического потенциала.
Потенциал Нернста
Рассмотрим простую систему, представляющую собой два отсека, содержащие раствор соли (например, KCl) и разделённые мембраной, которая пропускает только катион, в нашем случае К+.

Растворы находятся в равновесии, это означает, что электрохимические потенциалы ионов в обоих отсеках одинаковы. Математически это будет выражаться уравнением:
Это уравнение, учитывая, что давления и моляльные объёмы вещества в обоих отсеках одинаковы, позволяет нам рассчитать разность электрических потенциалов между отсеками:

Это уравнение называется уравнением Нернста. Если учесть значения констант перед знаком логарифма, и вместо натуральных логарифмов использовать десятичные, то эту формулу можно записать в виде:
https://pandia.ru/text/78/170/images/image020_2.jpg" width="459" height="268">
Осмотическое давление раствора зависит от количества растворенных ионов и температуры. В соответствии с уравнением Вант-Гоффа осмотическое давление (π) раствора прямо пропорционально концентрации (С) растворенного вещества и абсолютной температуре раствора (T):
π = iRTC,
где i - изотонический коэффициент, зависящий от степени диссоциации электролита и показывающий, во сколько раз увеличивается количество растворенных частиц при диссоциации молекул; для неэлектролитов i = l, для электролитов i > 1; R - газовая постоянная.
Активный транспорт - движение против градиента электрохимического потенциала, осуществляемое с затратой химической энергии за счёт гидролиза АТФ или переноса электрона по дыхательной цепи.
Выделяют первично-активный и вторично-активный транспорт.
Рис. - Активный перенос ионов при работе транспортных АТФ-аз.
Транспорт называется первично-активным , если он осуществляется белками-переносчиками (они ещё называются ионными насосами), источником энергии для которых служат АТР, пирофосфат или субстраты, окисляемые в электрон-транспортных цепях митохондрий, хлоропластов.
Типичный пример первично-активного транспорта - активный транспорт ионов с помощью АТФ-аз.
Вторично-активным (сопряженным) транспортом называют процесс переноса ионов через мембрану против градиента его концентрации за счет энергии электрохимического градиента других ионов. Сопряженный транспорт может осуществляться в режиме симпорта (оба иона переносятся через мембрану в одном направлении) или антипорта (ионы транспортируются в противоположных направлениях). Вторично-активный транспорт обеспечивает мембранный перенос моносахаридов, сахарозы, аминокислот, пептидов, анионов и ряда катионов. Для этой цели мембранные белки-переносчики чаще всего используют электрохимический градиент ионов водорода , создаваемый различными Н+-насосами.

Рис. - Сопряженный транспорт ионов и веществ через мембраны (Δφ - разность потенциалов, ΔрН - разность концентрации протонов)
Между пассивными и активными потоками в клетке существует взаимодействие, направленное на поддержание постоянства ионного состава клетки.
При блокировании энергетики клетки (пониженной температурой, ингибиторами, темнотой) интенсивность активного транспорта снижается, приток ионов из внешней среды уменьшается. Одновременно наблюдается возрастание электрического сопротивления мембраны в десятки раз. Это свидетельствует об уменьшении транспорта ионов по пассивным каналам, что предотвращает потерю ионов, находящихся в клетке.
ВВЕДЕНИЕ
Мембранный транспорт – транспорт веществ сквозь клеточную мембрану в клетку или из клетки, осуществляемый с помощью различных механизмов – простой диффузии, облегченной диффузии и активного транспорта.
Важнейшее свойство биологической мембраны состоит в ее способности пропускать в клетку и из нее различные вещества. Это имеет большое значение для саморегуляции и поддержания постоянного состава клетки. Такая функция клеточной мембраны выполняется благодаря избирательной проницаемости, т.е. способностью пропускать одни вещества и не пропускать другие. Легче всего проходят через липидный бислой неполярные молекулы с малой молекулярной массой (кислород, азот, бензол). Достаточно быстро проникают сквозь липидный бислой такие мелкие полярные молекулы, как углекислый газ, оксид азота, вода, мочевина. С заметной скоростью проходят через липидный бислой этанол и глицерин, а также стероиды и тиреоидные гормоны. Для более крупных полярных молекул (глюкоза, аминокислоты), а также для ионов липидный бислой практически непроницаем, так как его внутрення часть гидрофобна. Так, для воды коэффициент проницаемости (см/с) составляет около 10-2, для глицерина – 10-5, для глюкозы – 10-7, а для одновалентных ионов – меньше 10-10.
Перенос крупных полярных молекул и ионов происходит благодаря белкам-каналам или белкам-переносчикам. Так, в мембранах клеток существуют каналы для ионов натрия, калия и хлора, в мембранах многих клеток – водные каналы аквапорины, а также белки-переносчики для глюкозы, разных групп аминокислот и многих ионов. Активный и пассивный транспорт.
Мембраны формируют структуру клетки и осуществляют ее функции. Нарушение функций клеточной и внутриклеточной мембран лежит в основе необратимого повреждения клеток и, как следствие, развитие тяжелых заболеваний сердечно-сосудистой, нервной, эндокринной системы.
1. Основные факты о строении клеточной мембраны.
К клеточным мембранам относятся плазмолемма, кариолемма, мембраны митохондрий, ЭПС, аппарата Гольджи, лизосом, пероксисом. Общей чертой всех мембран клетки является то, что они представляют собой тонкие (6-10 нм) пласты липопротеиновой природы, (липиды в комплексе с белками). Основными химическими компонентами клеточных мембран являются липиды (40%) и белки (60%); кроме того, во многих мембранах обнаружены углеводы (5-10%).
Плазматическая мембранна окружает каждую клетку, определяет ее размер и обеспечивает сохранение различий между содержимым клетки и внешней средой. Мембрана служит высокоизбирательным фильтром и отвечает за активный транспорт веществ, то есть, поступление в клетку питательных веществ и вывод наружу вредных продуктов жизнедеятельности. Наконец, мембрана ответственна за восприятие внешних сигналов, позволяет клетке реагировать на внешние изменения. Все биологические мембраны представляют собой ансамбли липидных и белковых молекул, удерживаемых вместе с помощью нековалентных взаимодействий.
Основу любой молекулярной мембраны составляют молекулы липидов, образующих бислой. К липидам относится большая группа органических веществ, обладающих плохой растворимостью в воде (гидрофобность) и хорошей растворимостью в органических растворителях и жирах (липофильность). Состав липидов в разных мембранах неодинаков. Например, плазматическая мембрана, в отличие от мембран эндоплазматической сети и митохондрий обогощена холестерином. Характерными представителями липидов, встречающихся в клеточных мембранах, являются фосфолипиды (глицерофосфатиды), сфингомиелины и из стероидных липидов – холестерин.
Особенностью липидов является разделение их молекул на две функционально различные части: гидрофобные неполярные, не несущие зарядов («хвосты»), состоящие из жирных кислот, и гидрофильные, заряженные полярные «головки». Это определяет способность липидов самопроизвольно образовывать двухслойные (билипидные) мембранные структуры толщиной 5-7 нм.
Первые опыты, подтверждающие это, были проведены в 1925 году.
Формирование бислоя является особым свойством молекул липидов и реализуется даже вне клетки. Важнейшие свойства бислоя: способность к самосборке – текучесть – ассиметричность.
2. Общие представления о проницаемости.
Xарактеристика мембран, стенок сосудов и эпителиальных клеток, отражающая способность проводить химические вещества; различают активную (активный транспорт веществ) и пассивную П. (фагоцитоз
3. Перенос молекул через мембрану.
Так как внутренняя часть липидного слоя гидрофобна, он представляет собой практически непроницаемый барьер для большинства полярных молекул. Вследствие наличия этого барьера, предотвращается утечка содержимого клеток, однако из-за этого клетка была вынуждена создать специальные механизмы для транспорта растворимых в воде веществ через мембрану. Перенос малых водорастворимых молекул осуществляется при помощи специальных транспортных белков. Это особые трансмембранные белки, каждый из которых отвечает за транспорт определенных молекул или групп родственных молекул.
В клетках существуют также механизмы переноса через мембрану макромолекул (белков) и даже крупных частиц. Процесс поглощения макромолекул клеткой называется эндоцитозом. В общих чертах механизм его протекания таков: локальные участки плазматической мембраны впячиваются и замыкаются, образуя эндоцитозный пузырек, затем поглощенная частица обычно попадает в лизосомы и подвергается деградации.
3.1 Диффузия (лат. diffusio - распространение, растекание, рассеивание) - процесс переноса материи или энергии из области с высокой концентрацией в область с низкой концентрацией (против градиента концентрации). Самым известным примером диффузии является перемешивание газов или жидкостей (если в воду капнуть чернил, то жидкость через некоторое время станет равномерно окрашенной). Другой пример связан с твёрдым телом: если один конец стержня нагреть или электрически зарядить, распространяется тепло (или соответственно электрический ток) от горячей (заряженной) части к холодной (незаряженной) части. В случае металлического стержня тепловая диффузия развивается быстро, а ток протекает почти мгновенно. Если стержень изготовлен из синтетического материала, тепловая диффузия протекает медленно, а диффузия электрически заряженных частиц - очень медленно. Диффузия молекул протекает в общем ещё медленнее. Например, если кусочек сахара опустить на дно стакана с водой и воду не перемешивать, то пройдёт несколько недель, прежде чем раствор станет однородным. Ещё медленнее происходит диффузия одного твёрдого вещества в другое. Например, если медь покрыть золотом, то будет происходить диффузия золота в медь, но при нормальных условиях (комнатная температура и атмосферное давление) золотосодержащий слой достигнет толщины в несколько микрометров только через несколько тысяч лет.
Все виды диффузии подчиняются одинаковым законам. Скорость диффузии пропорциональна площади поперечного сечения образца, а также разности концентраций, температур или зарядов (в случае относительно небольших величин этих параметров). Так, тепло будет в четыре раза быстрее распространяться через стержень диаметром в два сантиметра, чем через стержень диаметром в один сантиметр. Это тепло будет распространяться быстрее, если перепад температур на одном сантиметре будет 10 °C вместо 5 °C. Скорость диффузии пропорциональна также параметру, характеризующему конкретный материал. В случае тепловой диффузии этот параметр называется теплопроводность, в случае потока электрических зарядов - электропроводность. Количество вещества, которое диффундирует в течение определённого времени, и расстояние, проходимое диффундирующим веществом, пропорциональны квадратному корню времени диффузии.
Диффузия представляет собой процесс на молекулярном уровне и определяется случайным характером движения отдельных молекул. Скорость диффузии в связи с этим пропорциональна средней скорости молекул. В случае газов средняя скорость малых молекул больше, а именно она обратно пропорциональна квадратному корню из массы молекулы и растёт с повышением температуры. Диффузионные процессы в твёрдых телах при высоких температурах часто находят практическое применение. Например, в определённых типах электронно-лучевых трубок (ЭЛТ) применяется металлический торий, продиффундировавший через металлический вольфрам при 2000 °C.
3.2 Уравнение Фика
В большинстве практических случаев вместо химического потенциала применяется концентрация C. Прямая замена µ на C становится некорректной в случае больших концентраций, так как химический потенциал связан с концентрацией по логарифмическому закону. Если не рассматривать такие случаи, то выше приведённую формулу можно заменить на следующую.